大学や研究所にて、すでに研究されている内容を医療応用する場合や、先にニーズや課題があり、その解決に向けて研究を開始する場合など、状況は多々あるかと思います。
この段階では、要素技術の確立に向けて基礎研究を重ねるフェーズですので、薬機法などはあまり気にしなくて問題ありません。しかし、この段階から対応しておいたほうがよい項目をまとめましたので、参考にされてください。
Contents
知財戦略
昨今、大学でも特許を取得される方が増えてきましたので、特筆すべき事項ではないかもしれませんが、医療系事業は収益化が見込めるまでの期間が約10年と長いため、その辺を考慮した知財戦略を考えていく必要があります。
特許申請のタイミング
特許申請や取得のタイミングは、下記3点を考えると整理しやすいです。弁理士の先生に早めの段階から相談することをお勧めします。
- ビジネスモデル
・知財を企業に売却したい
・自社で最終製品を製造販売していきたい - 競合の開発状況
・競争が苛烈で競合が多くいる
・参入障壁が高く他企業が気軽に参入してこられない - 上市(医療機器を発売すること)までの期間
・比較的早期に上市可能
・開発にかなりの時間を要する
学会発表・論文発表と特許出願の関係
特許を取得するためには「新規性」が不可欠です。出願前に研究内容の全部または一部を外部に公開(学会発表、論文投稿、Web公開、オープンな場での口頭発表など)してしまうと、その発表自体によって発明の新規性が失われ、特許が取れなくなる可能性があります。
一方で、研究者にとっては成果を早く公表し、優先権を示したいというニーズもあります。そこで日本の特許法では「新規性喪失の例外」(第30条)が設けられており、一定の条件を満たせば発表後でも新規性が保持されたものと扱われます。
一般に「学会発表後1年以内に出願すればよい」と言われるのはこの規定によるものです。
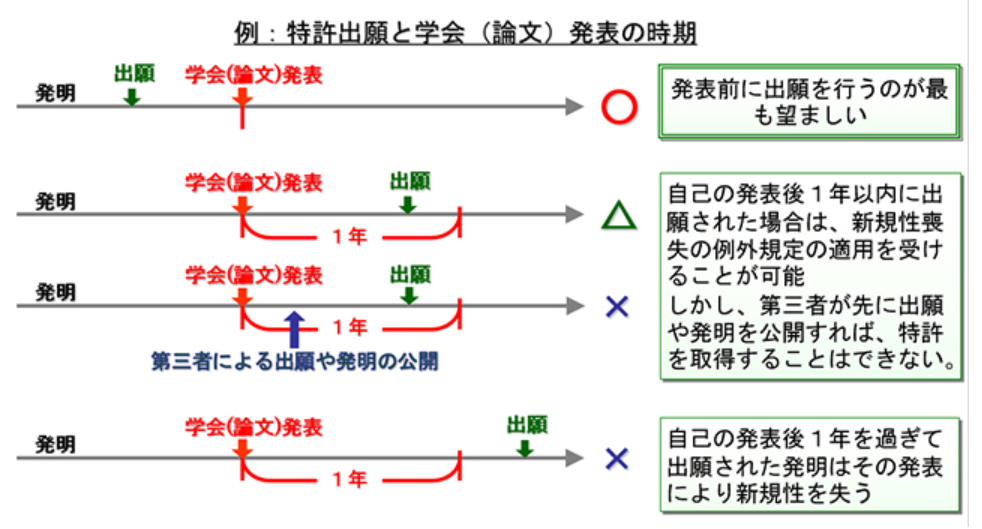
新規性喪失の例外を使うための主な条件
- 発明者自身(または権利を持つ者)が発表したこと
- 公開から1年以内に特許出願すること(予稿集の発行日も公表日に含まれます)
- 出願時に例外適用を希望する旨を届け出、出願後30日以内に証明書類を提出すること(複数回発表した場合はその都度手続きが必要)
注意点
- この例外は日本国内のみ有効です。外国で特許を取りたい場合、同様の制度がない国では「新規性を失った発明」とみなされることがあります。
- 発表内容をもとに他者が改良発明を行い、先に出願されてしまう可能性もあります。
実務上のポイント
学会発表や論文投稿の前に、可能な限り先に特許出願をしておくのが安全です。もし既に発表した内容について出願する場合は、例外適用の手続きを忘れずに行いましょう。
詳細な手続きは特許庁の公式ページを参照してください:
特許庁:発明の新規性喪失の例外制度
特許出願前に「公証」しておく必要性
公証とは
公証とは、文書の内容や作成日付、作成者などの事実を、公的な第三者(公証人役場や電子公証サービス)が証明することです。
紙の書面であれば「公証人役場で確定日付を取る」、デジタルデータであれば「電子公証・タイムスタンプを付与する」などの方法があり、これによって「その日時にその内容が存在していた」ことを後から客観的に証明できます。
公証のメリット
特許は出願するとその時点で権利が発生するわけではなく、審査を経て初めて権利化されます。また、出願書類に書いていないことは原則として保護されません。
そのため、発明の内容や発明した日付、誰が発明したかを客観的に証明できる「公証」やタイムスタンプを事前に取っておくことは、以下のようなメリットがあります。
- 優先権の証拠として使える
万一、他者が似た発明を先に出願・発表した場合でも、発明日を証明することで交渉材料や先使用権の主張に役立つことがあります。 - 共同研究・共同開発での紛争防止
誰がどのアイデアを出したかを公証しておくことで、後々の知財帰属トラブルを避けやすくなります。 - 特許出願の戦略立案に余裕が持てる
公証で証拠を確保したうえで、出願内容や範囲を慎重に検討することができます。
公証の方法としては、公証人役場での「確定日付」、電子公証サービス、タイムスタンプサービスなどがあります。
これらを使って、特許出願前の発明内容や発明日を第三者が確認できる形にしておくことが望ましいでしょう。
学会発表・論文投稿
医療機器開発に向けて公開しておいた方がよい情報もある
薬事承認の前だからといって、すべての情報を非公開にするのが最善とは限りません。機器の種類にもよりますが、要素技術の基盤となる生体や材料の物性データなどは、むしろ公表しておくことが有効な場合があります。
例えばX線画像装置では、組織に含まれる元素の種類や量によって「線吸収係数」が変化します。このとき、各組織ごとの線吸収係数が独自値のままだと、「その数値自体が正しいのか」という点から審査対象となり、開発や承認の過程が複雑になるリスクがあります。
一方で、こうした値を査読付き論文など第三者が認める形で公表しておけば、要素技術の根拠が公の事実として扱われ、審査でも揺らぎにくくなります。
さらに、こうした基礎データに人種差があるか否かについても事前に公表しておくと、将来的な海外展開の際に重要な裏付けとして活用できます。
プロトタイプの開発
医療機器開発におけるプロトタイプ(試作)は、最終製品をそのまま作ることが目的ではありません。まずは機能検証・コンセプト実証のための試作品として位置づけることが重要です。
なぜ最終製品を作らないのか
- 初期段階で最終製品レベルを目指すと、仕様が固定化されてしまい、柔軟な改良が難しくなります。
- 薬事・規格・ユーザー要求の検討が不十分な段階で「完成品」を作ると、後工程で大きな手戻りが発生しやすくなります。
プロトタイプ開発の目的
- 主要な機能・性能の確認
- ユーザー評価やフィードバックの取得
- 技術的・薬事的リスクの洗い出し
この段階では、外観や細部の仕上げよりも「原理が成り立つか」「安全性・性能が期待どおりか」に焦点を当てます。
体制構築準備
工学系の研究者の場合、研究に協力してくれる医師の方との関係性を構築しておいた方がよいです。臨床研究が今後必要になった場合や、PMDAとの相談において医師の見解が必要になった時など、技術を理解してくれている医師がいると盤石です。